Un nuovo studio giapponese individua il gene REDD2 come responsabile della distruzione delle cellule beta del pancreas in condizioni di stress metabolico. Un passo avanti nella diagnosi precoce e nella prevenzione del diabete.
C’è una guerra silenziosa che si consuma ogni giorno dentro di noi. Non è fatta di battaglie e fanfare, ma di stress, zuccheri in eccesso e scelte alimentari che lentamente, goccia dopo goccia, logorano ciò che ci mantiene in equilibrio: l’insulina. Ora, grazie a un nuovo studio dell’Università Metropolitana di Osaka, possiamo dare un nome al sabotatore interno: REDD2, un gene reattivo allo stress che, quando entra in azione, spinge le cellule pancreatiche verso l’autodistruzione.
Sì, hai letto bene: lo stress non fa male solo all’umore, ma può diventare il vero mandante dell’insorgenza del diabete di tipo 2, colpendo direttamente le cellule beta, quelle che hanno l’onere (e l’onore) di produrre insulina e tenere sotto controllo la glicemia.
Lo stress, il gene e il disastro cellulare
Secondo quanto affermato da Naoki Harada, professore associato alla Graduate School of Agriculture dell’ateneo nipponico, “le cellule beta subiscono un deterioramento sotto stress cronico causato da diete scorrette”, innescando una condizione nota come stress ossidativo. In questa situazione, il gene REDD2 si attiva come fosse un sistema di allarme… ma con effetti controproducenti.
Invece di proteggere, REDD2 si trasforma in carnefice: danneggia le cellule beta, riduce la loro capacità di secernere insulina e, col tempo, ne causa la morte. Un colpo basso al pancreas che apre le porte al diabete.
Cosa accade nel laboratorio (e nel nostro corpo)
Nel corso dello studio, i ricercatori hanno esposto le cellule beta a livelli elevati di glucosio, acidi grassi e STZ (una sostanza che simula il diabete nei test). Risultato? Aumento drastico dell’attività di REDD2. Ma c’è un “però”: quando il gene veniva silenziato, le cellule resistevano meglio allo stress e producevano più insulina.
I test su modelli murini confermano: i topi privi di REDD2, anche se nutriti con diete iperlipidiche o sottoposti a sostanze diabetogene, mantenevano un controllo glicemico ottimale. Non solo: avevano più cellule beta e più insulina in circolo. Un risultato che ha dell’incredibile.
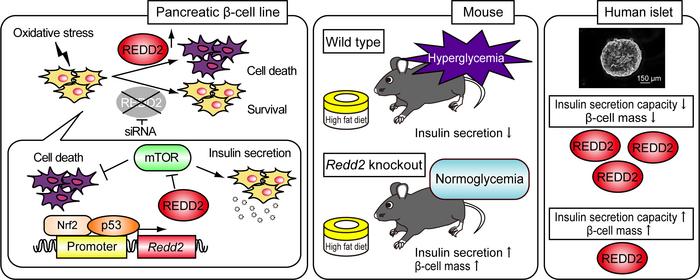
CREDITO
Università metropolitana di Osaka
Un nuovo orizzonte per la prevenzione
Questa scoperta non resta confinata alle provette. L’analisi delle isole pancreatiche umane ha mostrato lo stesso schema: livelli elevati di REDD2 corrispondono a una minore massa cellulare ? e a una secrezione insulinica ridotta.
Da qui, l’ipotesi audace ma concreta del team giapponese: REDD2 potrebbe diventare un marcatore diagnostico precoce del diabete di tipo 2, nonché un bersaglio per futuri farmaci o alimenti funzionali capaci di bloccarne l’attività prima che sia troppo tardi.
Come afferma Harada: “La soppressione dell’espressione di REDD2 protegge le cellule ? anche in condizioni di stress alimentare. Questo potrebbe rivoluzionare l’approccio alla prevenzione e al trattamento del diabete”.
Una battaglia quotidiana, ma non solitaria
Il diabete di tipo 2 non nasce da un giorno all’altro. È una conseguenza subdola di abitudini sbagliate, stress cronico, e scelte alimentari troppo ricche e troppo frequenti. Ma questa ricerca ci dice anche che possiamo invertire la rotta, a patto di ascoltare i segnali del corpo e della scienza.
REDD2 non è il nostro destino, ma un nemico che possiamo imparare a disinnescare. La prevenzione, l’alimentazione consapevole e – presto, forse – una terapia mirata, possono aiutarci a proteggere le cellule beta, difendendo la nostra capacità di produrre insulina e vivere meglio, più a lungo e con più consapevolezza.
Hashtag per i social
#DiabeteTipo2 #REDD2 #StressMetabolico #Insulina #CelluleBeta #PrevenzioneDiabete #RicercaScientifica #SalutePancreas #AlimentazioneConsapevole #JournalOfBiologicalChemistry

