Un team guidato da Maike Sander sviluppa per la prima volta un modello vascolarizzato di isole pancreatiche da cellule staminali: un passo avanti verso terapie più efficaci contro il diabete di tipo 1
C’è una rivoluzione silenziosa in corso nei laboratori del Max Delbrück Center, e riguarda uno dei misteri più intricati della medicina moderna: il diabete di tipo 1. Per la prima volta, un team internazionale di scienziati guidato dalla professoressa Maike Sander, Direttrice Scientifica del centro tedesco e ricercatrice presso l’Università della California a San Diego, ha sviluppato un modello vascolarizzato di isole pancreatiche da cellule staminali pluripotenti umane. Uno spartiacque scientifico pubblicato sulla prestigiosa rivista Developmental Cell.
Le isole pancreatiche – quei piccoli agglomerati cellulari che nel nostro corpo producono ormoni vitali come l’insulina – sono ora riprodotte in laboratorio in forma organoide, con una sofisticata rete di vasi sanguigni che ne migliora la maturazione e funzionalità. Una ricetta che, dopo cinque anni di sperimentazione, si è rivelata vincente grazie alla sapiente combinazione di cellule endoteliali, fibroblasti e un medium di coltura calibrato al micron.
“La nostra svolta è stata l’elaborazione della ricetta”, afferma Sander. “Non bastava riprodurre le cellule: dovevamo ricreare il contesto in cui esse si sviluppano, respirano, comunicano. Il microambiente è la chiave”.
I risultati sono sorprendenti: gli organoidi vascolarizzati hanno prodotto quantità significativamente superiori di insulina rispetto ai modelli tradizionali, dimostrando una maggiore maturità delle cellule beta, quelle più colpite dal diabete di tipo 1. Ma non finisce qui: grazie all’integrazione in dispositivi microfluidici, che simulano il flusso sanguigno, i ricercatori hanno osservato un’ulteriore accelerazione della maturazione cellulare.
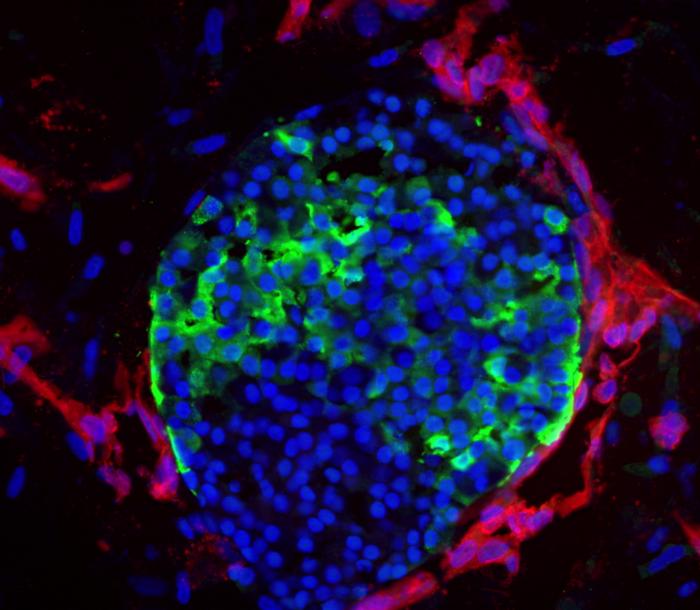
L’immagine mostra la vascolarizzazione (in rosso) che avvolge strettamente le cellule produttrici di insulina (in verde) negli isolotti (in blu).
Credito
Credito immagine: laboratorio Sander
Più vicini al pancreas reale
Nel laboratorio, i nuovi mini-organi sono diventati vere e proprie “isole” attive, capaci di rispondere al glucosio come farebbero nel corpo umano. È un passo avanti decisivo verso la comprensione di come queste cellule funzionano – e, soprattutto, come falliscono nei pazienti diabetici.
Due sono i meccanismi biologici che rendono questo modello così efficace. Primo: la formazione di una matrice extracellulare, ovvero un’impalcatura proteica che favorisce la crescita e la maturazione delle cellule. Secondo: la secrezione di proteina morfogenetica ossea (BMP) da parte delle cellule endoteliali, capace di stimolare la maturazione delle cellule beta.
“Abbiamo trovato un gradiente”, spiega Sander. “Più i modelli si avvicinavano all’ambiente naturale, più le cellule diventavano funzionali. È come se avessero bisogno di sentirsi a casa per fare il loro dovere”.
Un ponte verso la terapia cellulare
Il vero banco di prova, però, è stato l’esperimento in vivo. Topi diabetici trapiantati con isole SC vascolarizzate hanno mostrato risultati notevolmente migliori, con alcuni che non presentavano più segni di malattia anche dopo 19 settimane. Un dato che apre spiragli concreti per future terapie cellulari e per la cura del diabete in fase avanzata.
La pre-vascolarizzazione delle cellule prima del trapianto potrebbe diventare una prassi standard nella medicina rigenerativa del futuro. Non si tratta più solo di produrre cellule: si tratta di riprodurre l’intero ecosistema che le rende vive e attive.
Verso una nuova era nella ricerca sul diabete di tipo 1
Lo studio rappresenta anche un trampolino per lo studio delle dinamiche autoimmuni del diabete di tipo 1. Il team di Sander sta infatti coltivando organoidi vascolarizzati da cellule di pazienti diabetici, con l’obiettivo di osservare da vicino come le cellule immunitarie attaccano le cellule beta.
Un “teatro biologico” su chip, in cui immunologi, bioingegneri e clinici potranno studiare in tempo reale l’origine del caos autoimmune, e forse – un giorno – bloccarlo prima che distrugga il tessuto pancreatico.
Il Max Delbrück Center: dove la medicina del futuro prende forma
Il Max Delbrück Center, parte dell’Associazione Helmholtz, è tra le istituzioni europee più avanzate nella medicina molecolare. Con sedi a Berlino e Heidelberg, il centro conta 1.800 ricercatori da oltre 70 paesi, impegnati a decifrare i meccanismi più intimi della salute e della malattia. La filosofia è chiara: dalla scoperta alla cura, passando per la comprensione sistemica del corpo umano.
In un’epoca in cui il diabete colpisce centinaia di milioni di persone, questa scoperta apre nuovi scenari terapeutici, più precisi, più umani, più speranzosi. La strada è lunga, certo. Ma ora è illuminata.
Hashtag per i social media
#DiabeteTipo1 #CelluleStaminali #Organoidi #RicercaMedica #TerapiaCellulare #MaxDelbrückCenter #ScienzaDelFuturo #Biotecnologie #Insulina #SalutePancreatica #InnovazioneBiomedica

